T细胞“耗竭”之谜新解: 解锁持久抗癌免疫的关键
发布日期:2025-12-17 22:58 点击次数:108
在慢性感染和肿瘤微环境中,CD8+T细胞常常陷入一种功能进行性丧失的状态——“T细胞耗竭”。这不仅导致免疫系统无法有效清除病原体或癌细胞,也是当前免疫治疗面临的主要挑战之一。近年来,随着单细胞测序、表观遗传学和代谢组学等技术的发展,科学家对T细胞耗竭的调控网络有了更深刻的理解。
Nature Reviews Immunology近期发表的综述“Regulators of CD8+T cell exhaustion”系统梳理了这一领域的最新进展,揭示了从微环境信号到细胞内转录编程的多层次调控机制,并为开发新一代免疫疗法提供了方向。

一、耗竭不是“终点”,而是动态分化过程
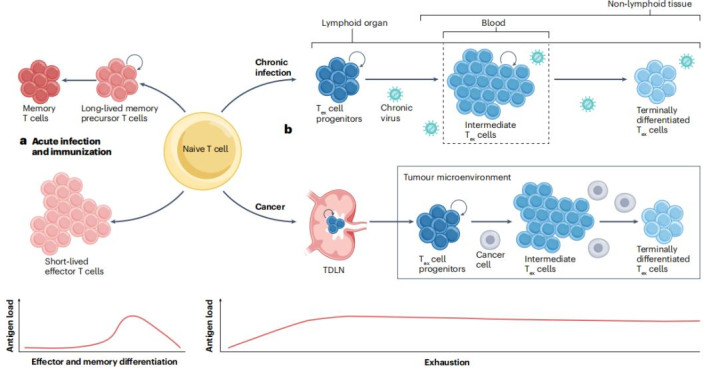
既往研究认为T细胞耗竭倾向于终末分化且难以逆转的功能障碍状态。新研究则指出,耗竭T细胞(Tex)存在明确的分化轨迹:从具有干细胞特性的前体细胞(progenitor Tex),到过渡态的中间耗竭细胞,最终分化为功能严重受损的终末耗竭细胞。
前体Tex细胞:以TCF1⁺PD-1⁺为特征,抑制性受体表达水平相对较低,具备干细胞样自我更新与增殖潜能。该亚群是免疫检查点抑制剂(如抗PD-1疗法)响应的核心细胞基础,主导治疗后的效应细胞再生。
终末Tex细胞:特征性高表达TIM-3、LAG-3等多类抑制性受体,增殖及效应细胞因子分泌能力显著受损,对现有免疫检查点阻断疗法的响应性极为有限。
这一发现意味着,治疗策略不应只关注“逆转耗竭”,更应聚焦于“维持前体细胞池”并引导其向功能性效应细胞分化。
二、微环境:耗竭的“推手”与“刹车”
Tex细胞的命运深受其所在微环境的调控,主要来自以下几方面:
1.抗原与共刺激/共抑制信号
持续性抗原刺激是驱动耗竭进程的核心因素。相比之下,低亲和力抗原或可控强度的TCR信号则有利于前体Tex细胞的维持与自我更新。
PD-1、CTLA-4、LAG-3等抑制性受体通过不同机制协同促进耗竭。例如,PD-1通过抑制CD28共刺激和IL-2信号,而LAG-3主要削弱TCR信号。联合阻断(如PD-1+LAG-3)已在临床中显示协同抗肿瘤效果。值得注意的是,这些受体在不同Tex亚群中的表达呈现时空异质性:PD-1在Tpex与效应样Tex细胞中广泛表达,而TIM-3与LAG-3则分别在终末与效应样亚群中富集,这决定了靶向治疗的亚群选择性。
CD28、4-1BB等共刺激信号则能增强Tex细胞的存活与功能,尤其是前体细胞的自我更新。
2. 细胞因子:双刃剑的智慧
细胞因子在耗竭调控中展现高度情境依赖性:
IL-2可促进效应分化,但持续高强度信号反而加速终末耗竭。
IL-10在慢性感染与肿瘤微环境中呈现双面调控特性:在慢性病毒感染中,高水平IL-10可抑制CD8⁺T细胞功能;而在特定实体瘤模型中,IL-10通过STAT3通路增强终末Tex细胞的氧化磷酸化水平及效应功能。这种功能异质性取决于IL-10表达剂量、受体分布模式及肿瘤微环境组成,需谨慎解读其治疗应用价值。
IL-21与IL-27等细胞因子对维持前体Tex细胞池及驱动其向效应样分化至关重要,在联合免疫治疗中展现出显著的协同增效潜力。
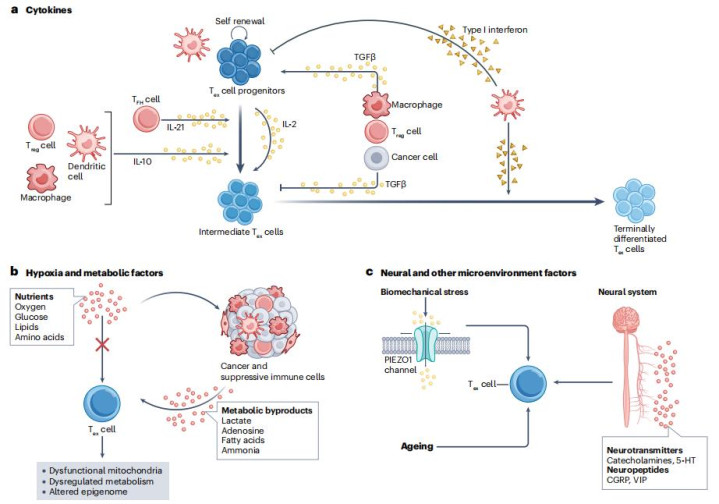
3. 代谢与缺氧:能量的博弈
肿瘤微环境常伴随缺氧、营养竞争及代谢废物堆积,直接重塑T细胞命运:
缺氧诱导HIF-1α,上调CD39/CD73–腺苷通路,强烈抑制T细胞功能。
葡萄糖、氨基酸匮乏削弱T细胞代谢适应性,而乳酸、氨等废物进一步加剧功能失调。
最新研究发现,在中性pH条件下的钠乳酸(而非酸性乳酸)可通过上调TCF1表达促进前体Tex细胞扩增,提示乳酸的免疫调控效应受其化学形态与微环境pH值共同调控。然而,该现象的具体机制及普适性仍需进一步验证。
4. 神经与机械信号:跨界调控
最新研究揭示了神经免疫交互在耗竭中的作用:
交感神经来源的儿茶酚胺通过β1-肾上腺素受体(ADRB1)信号通路,特异性抑制表达该受体的Tex细胞功能,加速耗竭进程。阻断该通路可显著提升免疫检查点阻断疗效。
肿瘤机械应力通过PIEZO1离子通道上调转录因子OSR2,加速终末耗竭。
这些发现为“神经–代谢–免疫”交互调控提供了新视角。
三、细胞内在编程:转录与表观遗传的“锁”
外部信号通过激活内部转录网络,驱动耗竭相关基因的稳定表达:
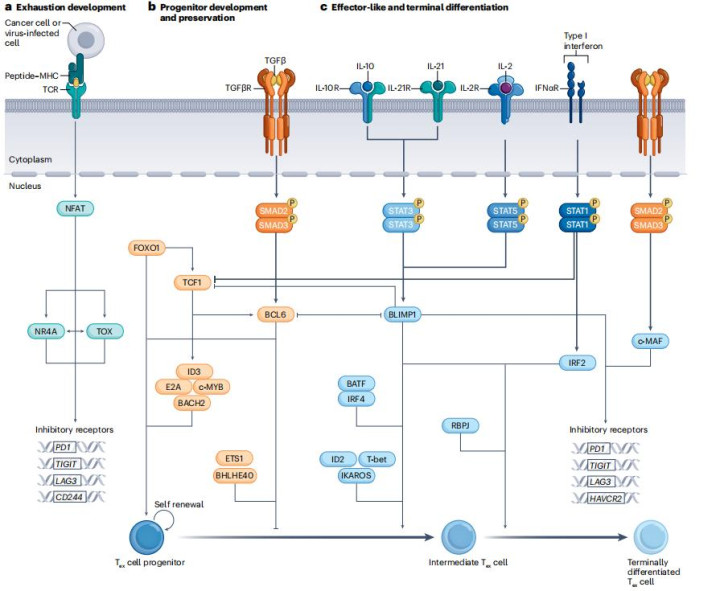
1.核心转录调控网络:
耗竭驱动因子:NFAT、NR4A及TOX在持续性抗原刺激下呈级联式激活。NFAT通过转录-表观遗传轴诱导NR4A与TOX表达,三者协同建立耗竭特异性表观遗传景观,稳定上调PD-1、TIM-3等抑制性受体,同时沉默效应分子基因。
干性维持因子:TCF1、BCL6、FOXO1等在Tpex细胞中优势表达。TCF1主导自我更新与增殖潜能维持;BCL6通过转录抑制BLIMP1等效应分化因子,阻滞终末耗竭进程;FOXO1则调控代谢适应性以支持长期存活。
效应/终末分化驱动因子:BLIMP1、T-bet、BATF等促进效应分化,但过度表达推动终末耗竭。
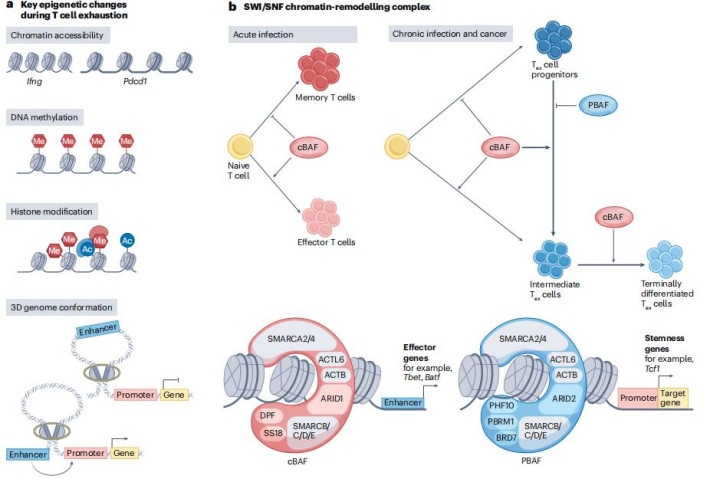
2.表观遗传“疤痕”
耗竭T细胞的染色质开放性、DNA甲基化、组蛋白修饰等发生持久性改变,形成“表观遗传记忆”,即使抗原清除后仍难以完全逆转。例如:
DNMT3A介导的从头DNA甲基化在Tex细胞激活后逐步建立,导致记忆相关基因座表观遗传沉默,显著削弱免疫检查点阻断介导的功能重振效果,形成"表观遗传疤痕"。
染色质重塑复合物BAF与PBAF分别推动效应分化与前体维持,成为潜在干预靶点。
四、治疗新策略:从“逆转耗竭”到“引导命运”
基于上述机制,新一代免疫疗法正朝多个方向突破:
联合检查点阻断:PD-1/CTLA-4双抗、PD-1/LAG-3联合疗法等已在临床试验中证实较单药治疗显著提升疗效,其机制与协同调控Tpex分化和逆转终末耗竭相关。
细胞因子工程:通过改变受体亲和力、靶向递送(如CD8导向的IL-2变体)等方式,精准调节T细胞分化。
代谢干预:补充乙酸、亚油酸等代谢物,或阻断腺苷、乳酸通路,改善T细胞功能。
表观遗传调控:使用DNMT3A、LSD1抑制剂或过表达AP-1因子(如c-Jun),重塑T细胞转录程序。
CAR-T/TCR-T优化:通过CRISPR敲除或PROTAC降解NR4A家族蛋白,或强制过表达FOXO1、AP-1家族成员(如c-Jun),可显著增强T细胞的干细胞特性、代谢适应性与抗肿瘤持久性,目前多项策略已进入早期临床试验阶段。
五、展望:迈向精准免疫重编程
T细胞耗竭是免疫系统在持续压力下的适应性反应,其调控网络复杂而动态。未来研究需进一步解析组织特异性微环境、细胞亚群异质性以及人体与模型差异,推动个体化治疗策略的发展。
展望未来,基于耗竭机制研究的新型免疫干预模式(包括体内CAR基因编辑、RNA药物及靶向递送系统)正成为转化研究热点。尽管文中未直接论述这些技术,但其揭示的Tpex调控节点为开发精准、可逆的T细胞重编程工具提供了理论基石。例如,通过mRNA编码工程化细胞因子或表观遗传调节因子,可实现体内精准、瞬时调控T细胞命运;而基于受体介导的靶向递送系统(如抗体-细胞因子融合蛋白)可实现对T细胞亚群的精准调控,在提升局部药效的同时降低脱靶毒性。
总结
T细胞耗竭的破解之路,正从单纯的“解除抑制”走向“多层次命运重编程”。在这一进程中,整合基因编辑、细胞工程、代谢调控与递送技术的创新型研发平台将成为推动下一代免疫治疗的关键。
百替生物作为聚焦细胞与基因治疗(CGT)创新的平台型企业,持续关注T细胞耗竭机制的前沿进展。我们致力于将该领域的科学发现转化为可及的临床解决方案,通过探索体内CAR mRNA药物及其递送系统技术,力求为肿瘤及慢性感染患者提供更有效的治疗选择。我们秉承科学严谨的态度,与学术界深度合作,共同推进免疫治疗从基础研究到临床应用的转化进程。

